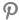미국 주요 PBM(처방약급여관리업체)들이 HLB의 간암신약을 올해 처방 예상목록에 연이어 등재하면서 미국 식품의약국(FDA)의 신약허가에 긍정적 신호가 켜졌다.
8일 HLB는 미국 3대 PBM 중 하나이자 전체 PBM 시장의 20% 이상을 차지하는 옵텀Rx, 서브유Rx 등 주요 PBM들이 리보세라닙과 캄렐리주맙을 '시판될 것으로 현저히 예상되는 의약품'(significant predicted forthcoming drug) 목록에 포함했다고 밝혔다.
PBM이란 미국 의료보험시장에서 의약품을 유통하는 처방약 관리업무 대행업체로, 여러 보험사와 계약해 의약품 목록을 선별·유지하고 약제비 청구 심사와 지급 등을 담당한다. PBM에 등재되지 않으면 미국 판매가 사실상 어렵기 때문에 미국에선 최대한 많은 PBM의 보험 등재목록에 등재되는 게 중요하다.
이에 따라 향후 FDA 신약허가를 받을 경우 HLB가 해당 PBM들은 물론 미국 내 여러 보험사 및 산하 PBM들과 진행할 협상도 순조로워질 것으로 보인다.
FDA는 리보세라닙 병용요법에 대해 늦어도 5월까지 신약허가 여부를 결정할 예정이다. 회사도 미국 자회사인 엘레바와 함께 빠른 보험등재를 위한 전략을 수립 중이다.
리보세라닙 병용요법은 글로벌 3상을 통해 역대 최장의 환자생존기간(22.1개월)을 입증해 간암치료 분야에서 신기원을 연 것으로 평가받고 있다. 그런 만큼 광범위한 보험 목록 등재는 물론 처방 우선순위 등재 협상에서도 우위를 점할 수 있을 것으로 기대되고 있다.
간암 1차 치료분야에서는 기존 항암제가 환자의 간기능이나 위장관출혈 등의 문제로 치료에 한계를 보이고 있는 반면, 리보세라닙 병용요법은 환자의 간기능 정도(ALBI 1,2등급)에 상관없이 환자의 전체생존기간(mOS)과 무진행생존기간(mPFS)에서 일관된 치료효과를 입증했고 위장관출혈 문제도 없어, 많은 간암 전문의들이 빠른 시판을 기다리고 있는 상황이다.
실제 미국 케이스웨스턴 리저브대학 아밋 마히팔(Amit Mahipal) 교수는 항암 전문 매체 'OncLive'와의 인터뷰에서 "리보세라닙 병용요법이 간암 1차 치료에 있어 획기적 치료법을 제시했다"며 "허가 후 표준치료제가 될 것"이라고 강조한 바 있다.
Copyright @ NEWSTREE All rights reserved.